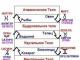
Механизм образования ковалентной связи. Механизм образования связи
Химическая связь.
Разные вещества имеют различное строение. Из всех известных на сегодняшний день веществ только инертные газы существуют в виде свободных (изолированных) атомов, что обусловлено высокой устойчивостью их электронных структур. Все другие вещества (а их в настоящее время известно более 10 млн.) состоят из связанных атомов.
Примечание: курсивом выделены те части текста, которые можно не учить и не разбирать.
Образование молекул из атомов приводит к выигрышу энергии, так как в обычных условиях молекулярное состояние устойчивее, чем атомное.
У атома на внешнем энергетическом уровне может содержаться от одного до восьми электронов. Если число электронов на внешнем уровне атома максимальное, которое он может вместить, то такой уровень называется завершенным . Завершенные уровни характеризуются большой прочностью. Таковы внешние уровни атомов благородных газов: у гелия на внешнем уровне два электрона (s 2), у остальных - по восемь электронов (ns 2 np 6). Внешние уровни атомов других элементов незавершенные и в процессе химического взаимодействия они завершаются.
Химическая связь образуется за счет валентных электронов, но осуществляется она по-разному. Различают три основных типа химических связей: ковалентную, ионную и металлическую.
Ковалентная связь
Механизм возникновения ковалентной связи рассмотрим на примере образования молекулы водорода:
Н + Н = Н 2 ; Q = 436 кДж
Ядро свободного атома водорода окружено сферически симметричным электронным облаком, образованным 1 s-электроном. При сближении атомов до определенного расстояния происходит частичное перекрывание их электронных облаков (орбиталей)
В результате между центрами обоих ядер возникает молекулярное двухэлектронное облако, обладающее максимальной электронной плотностью в пространстве между ядрами; увеличение же плотности отрицательного заряда благоприятствует сильному возрастанию сил притяжения между ядрами и молекулярным облаком.
Итак, ковалентная связь образуется в результате перекрывания электронных облаков атомов, сопровождающегося выделением энергии. Если у сблизившихся до касания атомов водорода расстояние между ядрами составляет 0,106 нм, то после перекрывания электронных облаков (образования молекулы Н 2) это расстояние составляет 0,074 нм. Наибольшее перекрывание электронных облаков осуществляется вдоль линии, соединяющей ядра двух атомов (это происходит при образовании σ–связи). Химическая связь тем прочнее, чем больше перекрывание электронных орбиталей. В результате возникновения химической связи между двумя атомами водорода каждый из них достигает электронной конфигурации атома благородного газа гелия.
Изображать химические связи принято по-разному:
1) с помощью электронов в виде точек, поставленных у химического знака элемента. Тогда образование молекулы водорода можно показать схемой
H∙ + H∙ →H:H
2) часто, особенно в органической химии, ковалентную связь изображают черточкой (штрихом) (например, Н-Н), которая символизирует общую пару электронов.
Ковалентная связь в молекуле хлора также осуществляется с помощью двух общих электронов, или электронной пары:
Неподеленная пара электронов, в атоме их 3
← Неподеленная пара электронов,
В молекуле их 6.
неспаренный электрон общая или поделенная пара электронов
Как видно, каждый атом хлора имеет три неподеленные пары и один неспаренный электрон. Образование химической связи происходит за счет неспаренных электронов каждого атома. Неспаренные электроны связываются в общую пару электронов, называемую также поделенной парой.
Если между атомами возникла одна ковалентная связь (одна общая электронная пара), то она называется одинарной; если больше, то кратной двойной (две общие электронные пары), тройной (три общие электронные пары).
Одинарная связь изображается одной черточкой (штрихом), двойная - двумя, тройная - тремя. Черточка между двумя атомами показывает, что у них пара электронов обобщена, в результате чего и образовалась химическая связь. С помощью таких черточек изображают структурные формулы молекул.
Итак, в молекуле хлора каждый его атом имеет завершенный внешний уровень из восьми электронов (s 2 p 6), причем два из них (электронная пара) в одинаковой мере принадлежат обоим атомам. Перекрывание электронных орбиталей при образовании молекулы показано на рис:
В молекуле азота N 2 атомы имеют три общие электронные пары:
:N· + ·N: → :N:::N:
Очевидно, молекула азота прочнее молекулы водорода или хлора, чем и обусловлена значительная инертность азота в химических реакциях.
Химическая связь, осуществляемая электронными парами, называется ковалентной.
Механизмы образования ковалентной связи.
Ковалентная связь образуется не только за счет перекрывания одноэлектронных облаков, - это обменный механизм образования ковалентной связи.
При обменном механизме атомы предоставляют в общее пользование одинаковое количество электронов.
Возможен и другой механизм ее образования - донорно-акцепторный. В этом случае химическая связь возникает за счет неподеленной электронной пары одного атома и свободной орбитали другого атома.
Рассмотрим в качестве примера механизм образования иона аммония NH 4 +
При взаимодействии аммиака с НСl происходит химическая реакция:
NH 3 + HCl = NH 4 Cl или в сокращенном ионном виде: NH 3 + Н + = NH 4 +
При этом в молекуле аммиака атом азота имеет неподеленную пару электронов (двухэлектронное облако):
Билет №11
Билет №12
Билет №13
Билет №14
Билет №15 .
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 11
Окислительно-восстановительные реакции. Степень окисления элемента. Примеры окислителей и восстановителей.
Метод валентных связей (МВС). Обменный и донорно-акцепторный механизмы образования ковалентной связи.
Ответ:
Окислительно-восстановительные реакции (ОВР) – реакции, которые идут с изменением с.о. атомов. Окисли́тельно-восстанови́тельные реа́кции - это химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующихся путём перераспределения электронов между атомом-окислителем и атомом-восстановителем.
Степень окисления (с.о.) – заряд, который приписывается атому, считая его ионом
Окислитель (Ox ) – принимает электроны.
Восстановитель (Red ) – отдает электроны
Ox 1 + Red 2 Red 1 +Ox 2
Ox1 + ne– → Red1
Cu2+ + 2e– → Cu0
CuSO 4 + Zn → ZnSO 4 + Cu
Red2 – ne– → Ox2
Zn0 – 2e– → Zn2+
Метод валентных связей
1927 Г. – Гейтлер и Лондон Квантово-механический расчет молекулы водорода

Механизмы образования связи
|
Обменный А + BА: В |
Донорно-акцепторный А: +ВА: В BF 3 + F – – : NH 3 + H + + |
Механизм образования ковалентной связи.
МВС позволяет различать три механизма образования ковалентной связи: обменный, донорно-акцепторный, дативный.
Обменный механизм. К нему относят те случаи образования химической связи, когда каждый из двух связываемых атомов выделяет для обобществления по одному электрону, как бы обмениваясь ими. Для связывания ядер двух атомов нужно, чтобы электроны находились в пространстве между ядрами. Эта область в молекуле называется областью связывания (область наиболее вероятного пребывания электронной пары в молекуле). Чтобы произошел обмен не спаренными электронами у атомов необходимо перекрывание атомных орбиталей. В этом и заключается действие обменного механизма образования ковалентной химической связи. Атомные орбитали могут перекрываться только в том случае, если они обладают одинаковыми свойствами симметрии относительно межъядерной оси.

|
|
Донорно-акцепторный и дативный механизмы.
Донорно-акцепторный механизм связан с передачей неподеленной пары электронов от одного атома на вакантную атомную орбиталь другого атома. Например, образование иона - :

Вакантная р-АО в атоме бора в молекуле BF 3 акцептирует пару электронов от фторид-иона (донор). В образовавшемся анионе четыре ковалентные связи В-F равноценны по длине и энергии. В исходной молекуле все три связи В-F образовались по обменному механизму.
Атомы, внешняя оболочка которых состоит только из s- или р-электронов, могут быть либо донорами, либо акцепторами неподеленной пары электронов. Атомы, у которых валентные электроны находятся и на d-АО, могут одновременно выступать и в роли доноров, и в роли акцепторов. Чтобы различить эти два механизма ввели понятия дативного механизма образования связи.
Экзаменационный билет № 12
Второй закон термодинамики. Энтропия, ее физический смысл и способы вычисления. Изменение энтропии системы как вероятностный критерий направления протекания процесса.
Осмос. Осмотическое давление. Закон Вант-Гоффа для растворов неэлектролитов.
Ответ:
Второй закон термодинамики

В изолированной системе самопроизвольный процесс возможен лишь при увеличении энтропии.
(метод валентных связей)
1. Обменный механизм заключается в спаривании двух электронов, принадлежащих разным атомам и имеющим противоположные спины. Его можно выразить следующей схемой:
2. Донорно-акцепторный механизм –образование химической связи за счет предоставления одним атомом в общее пользование пары электронов, а другим – свободной орбитали. Атом, предоставляющий электронную пару, называется донором , а атом, имеющий свободную орбиталь, – акцептором . Схема образования связи:
Для объяснения пространственного расположения атомов в молекуле используют теорию гибридизации Л. Полинга.
Гибридизацией называют процесс взаимодействия электронных орбиталей, их слияния, приводящий к выравниванию по форме и энергии.В зависимости от того, какие орбитали участвуют в образовании гибридных орбиталей, рассматривают различные типы гибридизации и пространственные конфигурации образовавшихся гибридных орбиталей (рис. 2).
Рис. 2. Пространственное расположение электронных
облаков для различных типов гибридизации.
sp-гибридизация: взаимодействуют одна s- и одна p-орбитали, в результате образуются две орбитали нового типа, которые называются sp-гибридными; эти орбитали имеют форму неправильной восмерки, оси их лежат на одной прямой, образуя угол 180 0 , молекула имеет линейное строение;
sp 2 -гибридизация: взаимодействуют одна s- и две p-орбитали, в результате чего образуются три орбитали нового типа, которые называются sp 2 -гибридными; оси этих орбиталей лежат в одной плоскости, углы между ними равны 120 0 , молекула имеет форму правильного треугольника;
sp 3 -гибридизация: взаимодействуют одна s- и три p- орбитали, в результате гибридизации образуются четыре новые sр 3 -гибридные орбитали, оси которых направлены от центра к вершинам тетраэдра, углы между осями равны 109 0 28′, молекула имеет тетраэдрическое строение.
В молекуле аммиака (NH 3) атом азота тоже находится в sp 3 -гибридном состоянии, три пары электронов являются общими с атомами водорода и участвуют в образовании связей, а одна электронная пара (неподеленная электронная пара ) принадлежит только атому азота. Для предсказания геометрии молекулы аммиака атом азота следует поместить в центр тетраэдра, атомы водорода – в три вершины, а неподеленную электронную пару – в четвертую вершину, таким образом, молекула аммиака имеет пирамидальную форму.
Аналогично можно рассмотреть строение молекулы воды . В ней две неподеленные электронные пары кислорода занимают две вершины тетраэдра, а две другие заняты атомами водорода, что приводит к угловой форме молекулы воды.
Неподеленная электронная пара образует более размытое «электронное облако», чем связывающая (обобществленная, общая), поэтому она занимает больший объем, приводя к уменьшению валентных углов по сравнению с тетраэдрическими.
Валентные электроны располагаются не только на s- и p-орбиталях, но и на d, последние также принимают участие в образовании гибридных орбиталей. Осуществляются два случая гибридизации с участием d-орбиталей : sp 3 d 2 и sp 3 d. В первом случае молекула реализует октаэдрическое строение, а во втором образуется тригональная бипирамида (табл.7).
Таблица 7
Геометрические конфигурации молекул
А – многовалентный атом; X – атомы, связанные с атомом А; n – число атомов X; E – неподеленная пара электронов; m – количество неподеленных электронных пар.
Металлическая связь . В отличие от ионных и ковалентных соединений металлы обладают высокой электропроводностью и теплопроводностью. Высокая электропроводность металлов указывает на то, что электроны свободно могут передвигаться во всем его объеме, т.е. металл можно рассматривать как кристалл, в узлах решетки которого расположены ионы, связанные электронами, находящимися в общем пользовании, т. е. в металлах имеет место сильно нелокализованная химическая связь. Совокупность электронов, обеспечивающих эту связь, называют электронным газом.
Более общий подход к представлению об ионных, ковалентных и металлических кристаллах можно получить, применяя представления метода молекулярных орбиталей.
Комплексные соединения
При рассмотрении видов химической связи отмечалось, что силы притяжения возникают не только между атомами, но и между молекулами и ионами. Такое взаимодействие может приводить к образованию новых более сложных комплексных (или координационных) соединений.
Комплексными называют соединения, имеющие в узлах кристаллической решетки агрегаты атомов (комплексы), способные к самостоятельному существованию в растворе и обладающие свойствами, отличными от свойств составляющих их частиц (атомов, ионов или молекул).
В молекуле комплексного соединения (например, K 4 ) различают следующие структурные элементы: ион-комплексообразователь (для данного комплекса Fe), координированные вокруг него присоединенные частицы – лиганды или адденды (CN -), составляющие вместе с комплексообразователем внутреннюю координационную сферу ( 4-), и остальные частицы, входящие во внешнюю координационную сферу (K +). При растворении комплексных соединений лиганды остаются в прочной связи с ионом-комплексообразователем, образуя почти не диссоциирующий комплексный ион. Число лигандов называется координационным числом (в случае K 4 координационное число равно 6). Координационное число определяется природой центрального атома и лигандов, а также соответствует наиболее симметричной геометрической конфигурации: 2 (линейная), 4 (тетраэдрическая или квадратная) и 6 (октаэдрическая конфигурация).
Характерными комплексообразователями являются катионы: Fe 2+ , Fe 3+ , Co 3+ , Co 2+ , Cu 2+ , Ag + , Cr 3+ , Ni 2+ . Способность к образованию комплексных соединений связана с электронным строением атомов. Особенно легко образуют комплексные ионы элементы d-семейства, например: Ag + , Au + , Cu 2+ , Hg 2+ , Zn 2+ , Fe 2+ , Cd 2+ , Fe 3+ , Co 3+ , Ni 2+ , Pt 2+ , Pt 4+ и др. Комплексообразователями могут быть А1 3+ и некоторые неметаллы, например, Si и В.
Лигандами могут служить как заряженные ионы: F - , ОН - , NO 3 - , NO 2 - , Cl - , Вг - , I - , CO 3 2- , CrO 4 2- , S 2 O 3 2- , CN - , PO 4 3- и др., так и электронейтральные полярные молекулы: NH 3 , Н 2 О, РН 3 , СО и др. Если все лиганды у комплексообразователя одинаковы, то комплексное соединение однородное ,например Cl 2 ; если лиганды разные, то соединение неоднородное ,например Cl. Между комплексообразователем и лигандами обычно устанавливаются координационные (донорно-акцепторные) связи. Они образуются в результате перекрывания заполненных электронами орбиталей лигандов вакантными орбиталями центрального атома. В комплексных соединениях донором является комплексообразователь, акцептором – лиганд.
Количество химических связей между комплексообразователем и лигандами определяет координационное число комплексообразователя. Характерные координационные числа: Cu + , Ag + ,Au + = 2; Cu 2+ ,Hg 2+ ,Pb 2+ ,Pt 2+ , Pd 2+ =4; Ni 2+ ,Ni 3+ ,Co 3+ ,А1 3+ = 4 или 6; Fe 2+ , Fe 3+ , Pt 4+ , Pd 4+ , Ti 4+ , Pb 4+ , Si 4+ =6.
Заряд комплексообразователя равен алгебраической сумме зарядов составляющих его ионов, например: 4- , x + 6(-1) = 4-; x = 2.
Входящие в состав комплексного иона нейтральные молекулы не оказывают влияния на заряд. Если вся внутренняя сфера заполнена только нейтральными молекулами, то заряд иона равен заряду комплексообразователя. Так, у иона 2+ заряд меди х = 2+. Заряд комплексного иона равен зарядам ионов, находящихся во внешней сфере. В K 4 заряд равен -4, так как во внешней сфере находятся 4 катиона К + , а молекула в целом электронейтральна.
Лиганды во внутренней сфере могут замещать друг друга при сохранении одного и того же координационного числа.
Классификация и номенклатура комплексных соединений. Сточки зрения заряда комплексной частицы все комплексные соединения можно разделить на катионные, анионные и нейтральные.
Катионные комплексы образуют катионы металлов, координирующие вокруг себя нейтральные или анионные лиганды, причем суммарный заряд лигандов меньше по абсолютной величине, чем степень окисления комплексообразователя, например Cl 3 . Катионные комплексные соединения помимо гидроксокомплексов и солей, могут быть кислотами, например H – гексафторсурьмяная кислота.
В анионных комплексах , напротив, лигандов-анионов такое число, что суммарный заряд комплексного аниона отрицателен, например . В анионных комплексах в качестве лигандов выступают гидроксид-анионы – это гидроксокомплексы (например Na 2 –тетрагидроксоцинкат калия), или анионы кислотных остатков – это ацидокомплексы (например K 3 – гексацианоферрат (III) калия).
Нейтральные комплексы могут быть нескольких видов: комплекс нейтрального атома металла с нейтральными лигандами (например Ni(CO) 4 – тетракарбонил никеля, [Сr(С 6 Н 6) 2 ] – дибензолхром). В нейтральных комплексах другого вида заряды комплексообразователя и лигандов уравновешивают друг друга (например, – хлорид гексаамминплатины (IV), – тринитротриамминкобальт).
Классифицировать комплексные соединения можно по природе лиганда. Среди соединений с нейтральными лигандами различают аквакомплексы, аммиакаты, карбонилы металлов. Комплексные соединения, содержащие в качестве лигандов молекулы воды, называют аквакомплексами . При кристаллизации вещества из раствора катион захватывает часть молекул воды, которые попадают в кристаллическую решетку соли. Такие вещества называются кристаллогидратами, например А1С1 3 · 6Н 2 О. Большинство кристаллогидратов представляет собой аквакомплексы, поэтому их точнее изображать в виде комплексной соли ([А1(Н 2 О) 6 ]С1 3 – хлорид гексаакваалюминия). Комплексные соединения с молекулами аммиака в качестве лиганда называют аммиакатами , например C1 4 – хлорид гексаамминплатины (IV). Карбонилами металлов называют комплексные соединения, в которых лигандами служат молекулы оксида углерода (II), например, – пентакарбонил железа, – тетракарбонил никеля.
Известны комплексные соединения с двумя комплексными ионами в молекуле, для которых существует явление координационной изомерии, которая связана с разным распределением лигандов между комплексообразователями, например: – гексанитрокобальтат (III) гексаамминникеля (III).
При составлении названия комплексного соединения применяются следующие правила:
1) если соединение является комплексной солью, то первым называется анион в именительном падеже, а затем катион в родительном падеже;
2) при названии комплексного иона сначала указываются лиганды, затем комплексообразователь;
3) молекулярные лиганды соответствуют названиям молекул (кроме воды и аммиака, для их обозначения применяются термины «аква» и «амин» );
4) к анионным лигандам добавляют окончание – о, например: F - – фторо, С1 - – хлоро, О 2 - – оксо, CNS - – родано, NO 3 - – нитрато, CN - – циано, SO 4 2- – сульфато, S 2 O 3 2- – тиосульфато, СО 3 2- – карбонато, РО 4 3- – фосфато, ОН - – гидроксо;
5) для обозначения количества лигандов используются греческие числительные: 2 – ди-, 3 – три-, 4 – тетра-, 5 – пента-, 6 – гекса-;
6) если комплексный ион – катион, то для названия комплексообразователя используют русское наименование элемента, если анион – латинское;
7) после названия комплексообразователя римской цифрой в круглых скобках указывают его степень окисления;
8) у нейтральных комплексов название центрального атома дается в именительном падеже, а его степень окисления не указывается.
Свойства комплексных соединений. Химические реакции с участием комплексных соединений разделяют на два типа:
1) внешнесферные – при их протекании комплексная частица остается неизменной (реакции обмена);
2) внутрисферные – при их протекании происходят изменения в степени окисления центрального атома, в строении лигандов или изменения в координационной сфере (уменьшение или увеличение координационного числа).
Одним из важнейших свойств комплексных соединений является их диссоциация в водных растворах. Большинство растворимых в воде ионных комплексов – сильные электролиты , они диссоциируют на внешнюю и внутреннюю сферы: K 4 ↔ 4K + + 4 - .
Комплексные ионы достаточно устойчивы, они являются слабыми электролитами , ступенчато отщепляя в водный раствор лиганды:
4 - ↔ 3- + CN - (число ступеней равно числу лигандов).
Если суммарный заряд частицы комплексного соединения равен нулю, то имеем молекулу неэлектролита, например .
При обменных реакциях комплексные ионы переходят из одних соединений в другие, не изменяя своего состава. Электролитическая диссоциация комплексных ионов подчиняется закону действующих масс и количественно характеризуется константой диссоциации, которая носит название константы нестойкости К н. Чем меньше константа нестойкости комплекса, тем в меньшей степени он распадается на ионы, тем устойчивее это соединение. У соединений, характеризуемых высокой К н, комплексные ионы неустойчивы, т. е. их практически нет в растворе, такие соединения являются двойными солями . Отличие между типичными представителями комплексных и двойных солейзаключается в том, что последние диссоци-ируют с образованием всех ионов, которые входят в состав этой соли, например: KA1(SO 4) 2 ↔ К + + А1 3+ + 2SO 4 2- (двойная соль);
К ↔ 4К + + 4- (комплексная соль).
Литература
1. Глинка Н. Л. Общая химия. – М.: Химия, 2006. – 720 с.
2. Глинка Н.Л. Задачи и упражнения по общей химии. – Л. Химия, 1985. – 264 с.