Параллельное предложение примеры. Химия
Одной молекулы и атомами водорода другой, типа Н-Х (Х - это F, O, N, Cl, Br, I) за счет сил электростатического притяжения.
Связь между водородом и одним из этих атомов характеризуется достаточной полярностью, поскольку связующее электронное облако смещено в сторону более электроотрицательного атома. Водород в данном случае расположен на положительном конце диполя. Два и более таких диполя взаимодействуют между собой так, что ядро атома водорода одной молекулы (положительный конец диполя) притягивается неподеленной электронной парой второй молекулы. Данная связь проявляется в газах, жидкостях и твердых телах.
Она относительно прочна. Наличие водородной связи обусловливает повышение устойчивости молекул вещества, а также повышению их температуры кипения и плавления. Образование водородных связей играет важную роль как в химических, так и в биологических системах.
Водородная связь бывает внутри- и межмолекулярной (рис. 14), молекулы карбоновых кислот в неполярных растворителях димеризуются за счет двух межмолекулярных водородных связей.
| а | б
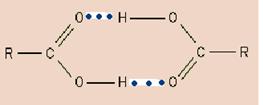 |
Рис. 14. Образование водородной связи: а - внутримолекулярной; б - межмолекулярной.
Существование веществ в различных агрегатных состояниях свидетельствует о том, что между частицами (атомы, ионы, молекулы) имеет место взаимодействие, обусловленное ван-дер-ваальсовыми силами притяжения. Наиболее важной и отличительной чертой этих сил является их универсальность, так как они действуют без исключения между всеми атомами и молекулами.
Водородные связи влияют на физические (т.кип. и т.пл., летучесть, вязкость, спектральные характеристики) и химические (кислотно-основные) свойства соединений.
Межмолекулярные водородные связи обусловливают ассоциацию молекул, что приводит к повышению температур кипения и плавления вещества. Например, этиловый спирт C 2 H 5 OH, способный к ассоциации, кипит при +78,3°С, а диметиловый эфир СН 3 ОСН 3 , не образующий водородных связей, лишь при 24°С (молекулярная формула обоих веществ С 2 Н 6 О).
Образование Н-связей с молекулами растворителя способствует улучшению растворимости. Так, метиловый и этиловый спирты (CH 3 OH, С 2 Н 5 ОН), образуя Н-связи с молекулами воды, неограниченно в ней растворяются.
Внутримолекулярная водородная связь образуется при благоприятном пространственном расположении в молекуле соответствующих групп атомов и специфически влияет на свойства. Например, Н-связь внутри молекул салициловой кислоты повышает ее кислотность.

Водородные связи и их влияние на свойства вещества
Также в настоящее время есть мнение, что водородная химическая связь бывает слабой и сильной.
Они отличаются друг от друга по энергии и длине связи (расстояние между атомами):
1. Водородные связи слабые. Энергия - 10-30 кДж/моль, длина связи - 30. Все вещества, перечисленные выше, являются примерами нормальной или слабой водородной связи.
2. Водородные связи сильные. Энергия - 400 кДж/моль, длина - 23-24.
Атом водорода, соединенный с атомом фтора, кислорода или азота (реже - хлора, серы или других неметаллов), может образовывать еще одну дополнительную связь. Это открытие, сделанное в восьмидесятых годах девятнадцатого столетия, связывают с именами русских химиков М.А. Ильинского и Н.Н. Бекетова . Было установлено, что некоторые водородсодержащие группы атомов часто образуют устойчивую химическую связь с электроотрицательными атомами, входящими в состав другой или той же самой молекулы. Такая химическая связь получила название водородной связи.
Водородная связь - это взаимодействие между двумя электроотрицательными атомами одной или разных молекул посредством атома водорода: А−Н ... В (чертой обозначена ковалентная связь, тремя точками - водородная связь).
Водородная связь обусловлена электростатическим притяжением атома водорода (несущим положительный заряд δ+) к атому электроотрицательного элемента, имеющего отрицательный заряд δ−. В большинстве случаев она слабее ковалентной, но существенно сильнее обычного притяжения молекул друг к другу в твердых и жидких веществах. В отличие от межмолекулярных взаимодействий водородная связь обладает свойствами направленности и насыщаемости, поэтому ее нередко считают одной из разновидностей ковалентной химической связи. Она может быть описана с помощью метода молекулярных орбиталей как трехцентровая двухэлектронная связь.
Одним из признаков водородной связи может служить расстояние между атомом водорода и другим атомом, ее образующим. Оно должно быть меньше, чем сумма радиусов этих атомов. Чаще встречаются несимметричные водородные связи, в которых расстояние Н ... В больше, чем А−В. Однако в редких случаях (фтороводород, некоторые карбоновые кислоты) водородная связь является симметричной. Угол между атомами во фрагменте А−Н ... В обычно близок к 180 o . Наиболее сильные водородные связи образуются с участием атомов фтора. В симметричном ионе − энергия водородная связи равна 155 кДж/моль и сопоставима с энергией ковалентной связи. Энергия водородная связи между молекулами воды уже заметно меньше (25 кДж/моль).
Межмолекулярная и внутримолекулярная водородная связь
Водородные связи обнаружены во многих химических соединениях. Они возникают, как правило, между атомами фтора, азота и кислорода (наиболее электроотрицательные элементы), реже - при участии атомов хлора, серы и других неметаллов. Прочные водородные связи образуются в таких жидких веществах, как вода, фтороводород, кислородсодержащие неорганические кислоты, карбоновые кислоты, фенолы, спирты, аммиак, амины. При кристаллизации водородные связи в этих веществах обычно сохраняются. Поэтому их кристаллические структуры имеют вид цепей (метанол), плоских двухмерных слоев (борная кислота), пространственных трехмерных сеток (лед).
Если водородная связь объединяет части одной молекулы, то говорят о внутримолекулярной водородной связи. Это особенно характерно для многих органических соединений (рис. 42). Если же водородная связь образуется между атомом водорода одной молекулы и атомом неметалла другой молекулы (межмолекулярная водородная связь), то молекулы образуют довольно прочные пары, цепочки, кольца. Так, муравьиная кислота и в жидком и в газообразном состоянии существует в виде димеров:
а газообразный фтороводород содержат полимерные молекулы, включающие до четырех частиц HF. Прочные связи между молекулами можно найти в воде, жидком аммиаке, спиртах. Необходимые для образования водородных связей атомы кислорода и азота содержат все углеводы, белки, нуклеиновые кислоты. Известно, например, что глюкоза, фруктоза и сахароза прекрасно растворимы в воде. Не последнюю роль в этом играют водородные связи, образующиеся в растворе между молекулами воды и многочисленными OH-группами углеводов.
Аномалии свойств, обусловленные наличием водородной связи
Наличием водородных связей обусловлены уникальные свойства многих веществ, в том числе воды. Трехатомная молекула Н 2 О образует четыре водородные связи. В их образовании принимают участие оба атома водорода, а атом кислорода, имеющий две неподеленные электронные пары, образует две водородные связи с атомами водорода соседних молекул воды.

Если бы не было водородных связей, то температуры плавления и кипения воды были бы существенно ниже, как это наблюдается у других водородных соединений неметаллов
Температуры кипения халькогеноводородов
| H 2 Te | H 2 Se | H 2 S | H 2 O | |
| t кип, o С | −2 | −42 | −60 | 100 |
Сильные водородные связи между молекулами воды препятствуют ее плавлению и испарению.
Водородные связи являются причиной и другого уникального свойства воды - при плавлении ее плотность возрастает. В структуре льда каждый атом кислорода связан через атомы водорода с четырьмя другими атомами кислорода - из других молекул воды. В результате образуется очень рыхлая "ажурная" структура. Вот почему лед такой легкий.
При плавлении льда около 10% водородных связей разрушается, и молекулы воды немного сближаются. Поэтому плотность жидкой воды при температуре плавления выше, чем плотность льда. Дальнейшее нагревание, с одной стороны, должно вызывать увеличение объема воды. Это происходит со всеми веществами.
Но, с другой стороны, водородные связи продолжают разрушаться, а это должно приводить к уменьшению объема воды. В результате плотность воды изменяется неравномерно. Наибольшее значение (1,00 г/мл) она имеет при температуре 4 o С. Такова зимняя температура вблизи дна пресноводных водоемов, где скапливается вода с максимальной плотностью.
При замерзании вода расширяется и занимает больший объем. Плотность льда (0,92 г/мл) - меньше, чем плотность жидкой воды. Поэтому лед плавает на поверхности воды. Если бы у льда была более высокая плотность, по мере замерзания он опускался бы на дно, что сделало бы жизнь в водоемах зимой невозможной.
Наличие водородных связей влияет и на кислотные свойства многих веществ. Фтороводородная кислота, в отличие от других галогеноводородных кислот является слабой так как атомы водорода связаны сразу с двумя атомами фтора, что препятствует их отщеплению (по той же причине большинство карбоновых кислот являются слабыми). Благодаря особо прочным водородным связям фтороводородная кислота - единственная одноосновная кислота, способная образовывать кислые соли, например NaHF 2 .
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
ХАРКІВСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ
ім. В.Н. Каразіна
Кафедра хімічного матеріалознавства
ВОДНЕВИЙ ЗВ"ЯЗОК В ДИМЕРІ HF
Курсова робота
студента гр. Х- 134
хімічного факультету
КОЛІСНИКА ОЛЕКСІЯ ВАСИЛЬОВИЧА
Науковий керівник
к.х.н., доцент
В.В. Іванов
ХАРКІВ 2010
введение
Интерес к олигомерам фторида водорода (димеру, тримеру) в последние десятилетия поистине велик. Объясняется это прежде всего той ролью, которую играет водородная связь при интерпретации, моделировании и прогнозировании свойств огромного класса веществ, представляющих непосредственный практический интерес (достаточно вспомнить о воде). Ассоциаты молекул фторида водорода рассматриваются как наиболее простые комплексы, компоненты которых удерживаются с помощью водородных связей, а димер (HF) 2 стоит первым в этом ряду.
Сейчас много известно о структуре димера фторида водорода по результатам экспериментальных исследований методами молекулярной спектроскопии и в газовой фазе, и в инертных средах матриц благородных газов. В последнем случае используется прием, позволяющий отделить интересующее соединение от других молекул инертным растворителем, например аргоном, чтобы предотвратить химические реакции или комплексообразование с другими частицами. По результатам этих исследований и был сделан вывод о стабильности соединения (HF) 2 и определены многие его параметры. Строение комплекса (HF) 2 в настоящее время изучают и теоретически методами компьютерного моделирования, причем предсказания теории претендуют на точность, вполне сопоставимую с экспериментальной.
1 ЛИТЕРАТУРНЫЙ ОБЗОР
1.1 Водородная связь
Представления об участии атома водорода в образовании двух химических связей (а не одной, как соответствовало бы его классической валентности) появились в конце XIX века (Ильинский, 1887 год) и начале XX века (Мур и Винмил, 1912 год; Хаггинс, 1919 год). Дальнейшее достаточно быстрое накопление экспериментальных данных, для объяснения которых эти представления оказались полезными, позволило не только привыкнуть к самому факту наличия водородной связи, но и дать некоторые разъяснения, по каким причинам она возникает, почему такого типа связь наиболее широко распространена именно для водородсодержащих соединений и не столь часто встречается у соединений, в которых соответствующие атомы водорода заменены на другие, например на атомы щелочных металлов .
Водородную связь относят к числу слабых химических взаимодействий. Энергия водородной связи обычно лежит в пределах от 10 до 30 кДж/моль, хотя иногда она достигает и сотен кДж/моль. Энергии обычных химических связей (ковалентных и ионных), как правило, заметно превышают 150 кДж/моль, достигая, например, для молекул азота или оксида углерода величин 900 кДж/моль и более . Тем не менее за последние полвека появилось четкое понимание исключительной роли слабых взаимодействий, прежде всего роли водородных связей в стабилизации конденсированных состояний многих простых молекулярных систем, например воды, фтороводорода, и, что самое существенное, в стабилизации биополимеров (нуклеиновых кислот, белков).
Водородные связи позволяют полимерным цепям соединяться в специфические трехмерные структуры, приобретающие при этом функциональную биологическую активность, структуры, с одной стороны достаточно прочные (за счет образования большого числа водородных связей), а с другой - достаточно чутко реагирующие на изменение внешних условий (например, приближение той или иной молекулы) именно из-за того, что эти взаимодействия являются слабыми. Разрыв таких связей лишает белки или нуклеиновые кислоты их биологических функций. Отсюда, в частности, видна исключительно важная роль водородных связей, которую они играют в биологических процессах на молекулярном уровне . Понятно и то важное значение исследований и понимания природы водородных связей, которым в последние время было уделено столь пристальное внимание ученых различных направлений.
Долгое время доминировала сугубо электростатическая точка зрения: атом водорода, образующий такую связь, обычно связан с достаточно хорошо выраженным электроотрицательным атомом, то есть атомом с высоким сродством к электрону, из-за чего электронная плотность на атоме водорода понижена по сравнению с плотностью изолированного атома водорода. Следовательно, суммарный электрический заряд на таком атоме оказывается положительным, что и позволяет атому взаимодействовать еще с одним электроотрицательным атомом. Такое взаимодействие с каждым из двух атомов, как правило, слабее взаимодействия с тем атомом, с которым атом водорода был соединен первоначально. Образование подобной связи с третьим и т. д. атомом практически оказывается невозможным из-за того, что начинает доминировать электростатическое отталкивание электроотрицательных атомов друг от друга . Современные расчеты показывают, однако, что суммарный заряд на атоме водорода, участвующем в образовании водородной связи, практически не меняется по сравнению с зарядом в мономерной молекуле, что говорит о том, какую заметную роль в образовании водородной связи должны играть поляризация, перераспределение электронного заряда в отдельных областях пространства.
В настоящее время интерпретация образования химической связи дается, как правило, на языке теории молекулярных орбиталей, то есть в предположении, что для описания электронной структуры молекулы достаточно хорошим является приближение, когда каждый электрон задается своей одноэлектронной функцией, своей орбиталью.
Общей причиной возникновения водородной связи, как, впрочем, и других выделяемых обычно типов химических связей, является главным образом электростатическое, кулоновское взаимодействие разноименных зарядов тех частиц, которые образуют молекулу. Правда, это взаимодействие отличается от того, которое встречается в классической теории, поскольку оно не определяется только лишь плотностью распределения положительного и отрицательного зарядов, а выражается более сложным образом с помощью волновых функций, определяющих состояния молекулярной системы . Поэтому естественно стремление найти некоторые более простые образы, которые давали бы возможность наглядно представить себе, как же все-таки образуется химическая связь.
Одно из таких представлений базируется на анализе перераспределения электронной плотности при образовании системы: увеличение электронной плотности в пространстве между ядрами ведет к усилению электростатического взаимодействия между электронами в этом пространстве и ядрами, что сопровождается, в свою очередь, понижением энергии системы .
Действительно, такое повышение электронной плотности должно сопровождаться ее понижением в других областях пространства и, следовательно, вклад в энергию от этих областей должен уменьшаться . Кроме того, электроны, находясь в сравнительно малой указанной области пространства, должны сильнее отталкиваться друг от друга, а потому энергия также должна возрастать.
Анализ изменений распределения электронной плотности - полезный способ выяснения того, что происходит при возникновении химической связи. Простые представления не всегда оказываются работоспособными. Так, в настоящее время известны молекулы, в которых при образовании химической связи не происходит увеличения электронной плотности в пространстве между ядрами и тем не менее химическая связь вполне реально существует .
Водородная связь по своему происхождению не представляет собой нечто отличающееся от того, что характерно для химических связей вообще. Ее определяют главным образом поляризация электронного распределения в мономерных звеньях (в общем случае в молекулах, образующих такую связь) и отличная от мономерных звеньев динамика колебательного движения атомов в водородно-связанном фрагменте. Пристальное внимание к изучению систем с водородными связями давно уже определяется не спецификой этой связи как таковой, а широкой распространенностью водородных связей, особенно в биологических объектах, и той важной ролью, которую они играют в биополимерах и жизненно важных процессах с их участием .
1.2 Примеры соединений с водородной связью
Во многих случаях, когда имеется сильная связь между молекулами или разными группами одной и той же молекулы, эту связь можно приписать атомам водорода, проявляющим двухвалентный характер. Таковы, например, димеры алифатических кислот, ион дифторида
и димер HF, структура которых приведена на рисунке 1.1 .
Рисунок 1.1 Некоторые примеры структур с водородной связью
Водород служит в качестве связующего атома в другом важном классе соединений – бороводородах. Простейшим членом этого семейства является диборан (В 2 Н 6). Однако бороводороды обычно не рассматривают в качестве соединений с водородной связью, так как их нельзя разбить на фрагменты, представляющие собой стабильные молекулы . Рассмотрим эти соединения лишь для того, чтобы сопоставить их с комплексами с водородной связью.
Бороводороды были названы электронодефицитнымимолекулами (термин электронодефицитный в применении к бороводородам не совсем оправдан, так как во всех случаях электронов достаточно для заполнения всех связывающих молекулярных орбиталей), так как они не имеют достаточно электронов для образования того количества двухэлектронных связей, которое, по-видимому, подразумевается их молекулярной геометрией. Диборан имеет восемь связей В–Н, но только четырнадцать валентных электронов. Расчеты на основе метода молекулярных орбиталей показывают, что концевые связи представляют собой нормальные двухэлектронные связи, а мостиковые связи следует описывать как трехцентровые двухэлектронные связи .
Описание на основе метода молекулярных орбиталей иона дифторида полностью отличается от описания диборана, поскольку для образования мостиковых связей здесь имеются четыре электрона. Равновесная конфигурация молекулы линейная, причем водород находится посредине отрезка F–F. Две наивысшие заполненные молекулярные орбитали образованы в основном 2p σ -орбиталями фтора п ls -орбиталями водорода с некоторой добавкой 2s -орбиталей фтора. Низшая из двух орбиталей имеет симметрию σ g и является связывающей для всех трех атомов. Более высокая орбиталь σ u (ее узел приходится на атом водорода) – разрыхляющая по отношению к атомам фтора. Однако атомы фтора достаточно удалены друг от друга, так что разрыхляющий эффект мал, и орбиталь σ u имеет отрицательную энергию (т. е. связывает электроны), что обусловлено большой электроотрицательностью атома фтора .
Можно преобразовать σ g - и σ u -орбитали в эквивалентные орбитали θ 1 = σ g + σ u и θ 2 = σ g – σ u , локализованные на двух связях F–Н, что демонстрирует отличие от мостиков в бороводородах, орбитали которых не могут быть локализованы на связях .
Ион дифторида не типичен для соединений с водородными связями в том отношении, что атом водорода расположен посредине между двумя тяжелыми атомами. Обычно энергии водородных связей намного меньше, чем для иона дифторида, а водород более тесно связан с одним из атомов, чем с другим, как в димере муравьиной кислоты (рис. 1.1). В действительности геометрия двух компонентов, составляющих комплекс, немного отличается от их геометрии в изолированных состояниях .
Таблица 1.1 Энергии димеризации некоторых газофазных димеров с водородной связью
1.3 Димер HF
1.3.1 Геометрическая конфигурация, колебания, энергия связи
На рисунке 1.2 изображена равновесная геометрическая конфигурация комплекса, одновременно и понятная и непредсказуемая. Все четыре атома располагаются в одной плоскости. Расстояния между атомами фтора и водорода, относящиеся к составным (мономерным) частям комплекса F b –H b и F f –H f , равны соответственно 0,922 и 0,920 Å и мало отличаются от равновесного расстояния 0,917 Å в молекуле HF. Расстояние между атомами H b …Ff равно 1,82 Å, что характерно для водородной связи. Расположение всех трех участников водородной связи F b –H b …F f близко к линейному. Это все предсказуемые черты межмолекулярного комплекса с водородной связью. Непредсказуемыми из простых принципов оказываются значения углов θ 1 = 7 ̊ (между направлениями F b F f и F f H b) и θ 2 = 69 ̊ (F b F f и F f H f).

Рисунок 1.2 Равновесная геометрическая конфигурация комплекса (HF) 2
Рассмотрим, как были получены эти результаты. Олигомеры фторида водорода (HF) n образуются в распространяющейся со сверхзвуковой скоростью струе газа, истекающей из узкого сопла контейнера с веществом HF, находящегося при низких температурах. Контроль состава газа осуществляют масс-спектральными методами , что позволяет различить компоненты газа по массе, то есть различить олигомеры с разными значениями n. Подбором условий можно добиться того, чтобы исследованию подвергались именно димерные комплексы (HF) 2 .
В камере спектрометра молекулярный пучок подвергается действию электромагнитного излучения от источника определенного интервала длин волн (или частот) и фиксируется спектр исследуемой системы. Спектральные линии в микроволновом диапазоне, как сказано выше, несут информацию о вращении молекулы, и относительное расположение полос зависит от геометрической конфигурации системы. Интерпретация полос в диапазоне 19 300-19 340 МГц в рамках модели полужесткого волчка позволила установить соответствие спектра структуре, показанной на рис. 1, с расстоянием между атомами фтора Fb-Ff 2,72 ? 0,03 Б и углами q1 = 10 ? 6? и q2 = 63 ? 6?. Близкие значения углов были независимо получены и в другой лаборатории: q1 = 7 ? 3? и q2 = 60 ? 2?.
В следующих сериях экспериментов исследовали инфракрасный (ИК) диапазон спектра. Согласно основным моделям теории строения молекул, расположение спектральных линий в этой области несет информацию о колебаниях частиц молекулы около положения равновесия, в данном случае о небольших периодических смещениях атомов от позиций, показанных на рис. 1. Для каждой молекулы число таких колебаний однозначно определяется числом атомов и для комплекса (HF)2 оно равно шести. В молекулярной спектроскопии принято выражать частоты колебаний в единицах, показывающих число полных волн данной длины, укладывающихся на расстоянии в 1 см, и соответственно говорят о величинах частот, выраженных в обратных сантиметрах (см-1), или, что то же самое, в волновых числах. Хотя в каждом колебании с данной частотой принимают участие в той или иной мере все атомы молекулы, опять-таки в рамках модельных представлений можно отнести колебание (и соответственно полосу в ИК-спектре) к выделенной группе атомов. Во многих случаях такому подразделению способствуют значительные различия в частотах колебаний, как в нашем примере (HF)2 .
Оцененные по измерениям спектральных полос в газовой фазе и инертных матрицах частоты колебаний димера фторида водорода явно разделяются на внутримолекулярные (имеются в виду колебания молекул, при ассоциации которых образовался комплекс) с величинами около 4000 см-1 и межмолекулярные с величинами менее 500 см-1. Высокие частоты относятся к колебаниям групп Ff-Hf (3931 см-1) и Fb-Hb (3868 см-1). Низкие частоты (475, 395, 161 и 125 см-1) характеризуют колебания, меняющие относительную ориентацию фрагментов Ff-Hf и Fb-Hb , выход атомов из плоскости и изменения расстояния Fb_Ff .
Интенсивность ИК-линий можно связать (снова в рамках определенной модели молекулы) с такой важнейшей характеристикой комплекса, как энергия диссоциации на две мономерные молекулы. Эта же величина определяет энергию связи комплекса. По экспериментальным данным, она составляет 19,35 ? 0,71 кДж/моль. Таким образом, расшифровка спектров приводит к набору молекулярных постоянных - расстояниям между атомами, углам, частотам колебаний, энергиям, которые достаточно полно характеризуют строение молекулярной системы.
Обратимся теперь к теоретическому подходу. Все построения основаны на модели, согласно которой комплекс (HF)2 есть система четырех ядер (двух протонов и двух ядер F9 +) и 20 электронов, то есть точечных частиц, попарно взаимодействующих по закону Кулона. Больше никакой исходной информации в модель не закладывается, что и делает такие расчеты свойств молекул столь привлекательными. Для этой конкретной системы четырех ядер и 20 электронов методами вычислительной квантовой химии рассчитывают поверхность потенциальной энергии - зависимость энергии от координат ядер . Конечно, необходим доступ к компьютерам и достаточно сложному программному обеспечению, однако сейчас для такой системы, как (HF)2 , очень хорошие результаты можно получать с персональным компьютером типа "Pentium" за вполне реальное время, хотя требуются терпение и определенные навыки.
Одним из результатов компьютерного расчета является массив точек: энергия как функция в данном случае шести внутренних координат комплекса (HF)2 (число внутренних координат совпадает с числом колебательных степеней свободы молекулярной системы). Рельеф этой шестимерной поверхности достаточно сложный, с минимумами, максимумами, седловыми точками. Представление о двумерном сечении потенциальной поверхности основного электронного состояния в зависимости от угловых координат q1 и q2 дает рис. 2, причем все остальные геометрические переменные подстроены так, чтобы значения энергии для них были минимальными. На рис. 2 изображены рассчитанные контуры изоэнергетических линий, за нуль отсчета принята энергия разделенных молекул мономеров HF, синим цветом отмечены области отрицательных энергий, где комплекс (HF)2 существует как единое целое, красным - область положительных энергий. Изоэнергетические контуры сгущаются около стационарных точек - минимумов, седловых точек. Координаты точки наиболее глубокого минимума (темно-синий цвет на рис. 2 около | q1 | = 7?, q2 = 69?) определяют равновесную геометрическую конфигурацию комплекса. Рис. 2 симметричен относительно диагонали поля графика, что отражает эквивалентность двух структур комплекса
На рис. 1 показаны те значения координат, которые были получены в наиболее совершенном в настоящее время квантово-химическом расчете. Выше приведены величины, определенные из экспериментов, и согласие результатов обоих подходов к исследованию комплекса (HF)2 можно считать великолепным. Из расчета определяются и энергия связи по разности энергий в равновесной геометрической конфигурации (HF)2 и энергии двух невзаимодействующих молекул HF. Наилучшее полученное значение (19,23 кДж/моль) также прекрасно согласуется с экспериментально определенной энергией (19,35 ? 0,71 кДж/моль).
Еще одна серия экспериментальных данных позволила определить частоты колебаний комплекса. Решение колебательной задачи представляет следующий этап моделирования структуры молекул после построения поверхности потенциальной энергии. В простейшем приближении необходимо определить кривизну потенциальной поверхности по отношению ко всем внутренним координатам около положения минимума и оценить тем самым коэффициенты жесткости пружинок, моделирующих колебания вдоль связей и углов молекулы. Совокупность коэффициентов жесткости, рассчитываемых как вторые производные энергии по координатам, образует силовое поле молекулы. Далее по известным массам атомов, равновесным геометрическим параметрам и силовому полю без особого труда вычисляется набор частот колебаний. Для комплекса (HF)2 такая задача решалась неоднократно, и вычисленные частоты хорошо совпадают с экспериментальными.
Список литературы
1. Водородная связь / Ред. Н. Д. Соколов. М.: Наука, 1989.
2. Овчинников Ю. А. Биоорганическая химия. – М.: Просвещение, 1987. – 815 с.: ил.
3. Витковская Н. М. Метод молекулярных орбиталей: Основные идеи и важные следствия // Соросовский Образовательный Журнал. 1996. № 6. С. 58-64.
4. Степанов Н. Ф. Химическая связь в простых двухатомных молекулах // Соросовский Образовательный Журнал. 1998. № 10. С. 37-43.
5. Степанов Н. Ф. Потенциальные поверхности и химические реакции // Соросовский Образовательный Журнал. 1996. № 10. С. 33-41.
6. Маррел Дж., Кеттл С.,Теддер Дж. Химическая связь. М.: Мир, 1980. 384 с.
7. Немухин А. В. Димер фторида водорода: Строение простейшего комплекса с водородной связью // Соросовский Образовательный Журнал. 1998. № 7. С. 65-69.
8. Вилков Л. В. Физические методы исследования в химии // Соросовский Образовательный Журнал. 1996. № 5. С. 35-40.
9. Некрасов Б. В. Общая химия. М.: Госхимиздат, 1962. 973 с.
10. Салем Л.Электроны в химических реакциях. М.: Мир, 1985. 285 с.
11. Хобза П., Заградник Р. Межмолекулярные комплексы. М.: Мир, 1989. 376 с.
12. Немухин А. В., Вейнхольд Ф. Концепция Льюиса в современной квантовой химии // Рос. хим. журн. (Журн. Рос. хим. о-ва им. Д.И. Мендделеева). 1994. Т. 38. С. 5-11.
13. Немухин А. В. Многообразие кластеров // Соросовский Образовательный Журнал. 1996. Т. 40. С. 48-56.
1.2 Примеры соединений с водородной связью
Во многих случаях, когда имеется сильная связь между молекулами или разными группами одной и той же молекулы, эту связь можно приписать атомам водорода, проявляющим двухвалентный характер. Таковы, например, димеры алифатических кислот, ион дифторида и димер HF, структура которых приведена на рисунке 1.1 .

Рисунок 1.1 Некоторые примеры структур с водородной связью
Водород служит в качестве связующего атома в другом важном классе соединений – бороводородах. Простейшим членом этого семейства является диборан (В 2 Н 6). Однако бороводороды обычно не рассматривают в качестве соединений с водородной связью, так как их нельзя разбить на фрагменты, представляющие собой стабильные молекулы . Рассмотрим эти соединения лишь для того, чтобы сопоставить их с комплексами с водородной связью.
Бороводороды были названы электронодефицитными молекулами (термин электронодефицитный в применении к бороводородам не совсем оправдан, так как во всех случаях электронов достаточно для заполнения всех связывающих молекулярных орбиталей), так как они не имеют достаточно электронов для образования того количества двухэлектронных связей, которое, по-видимому, подразумевается их молекулярной геометрией. Диборан имеет восемь связей В–Н, но только четырнадцать валентных электронов. Расчеты на основе метода молекулярных орбиталей показывают, что концевые связи представляют собой нормальные двухэлектронные связи, а мостиковые связи следует описывать как трехцентровые двухэлектронные связи .
Описание на основе метода молекулярных орбиталей иона дифторида полностью отличается от описания диборана, поскольку для образования мостиковых связей здесь имеются четыре электрона. Равновесная конфигурация молекулы линейная, причем водород находится посредине отрезка F–F. Две наивысшие заполненные молекулярные орбитали образованы в основном 2pσ -орбиталями фтора п ls-орбиталями водорода с некоторой добавкой 2s-орбиталей фтора. Низшая из двух орбиталей имеет симметрию σ g и является связывающей для всех трех атомов. Более высокая орбиталь σ u (ее узел приходится на атом водорода) – разрыхляющая по отношению к атомам фтора. Однако атомы фтора достаточно удалены друг от друга, так что разрыхляющий эффект мал, и орбиталь σ u имеет отрицательную энергию (т. е. связывает электроны), что обусловлено большой электроотрицательностью атома фтора .
Можно преобразовать σ g - и σ u -орбитали в эквивалентные орбитали θ 1 = σ g + σ u и θ 2 = σ g – σ u , локализованные на двух связях F–Н, что демонстрирует отличие от мостиков в бороводородах, орбитали которых не могут быть локализованы на связях .
Ион дифторида не типичен для соединений с водородными связями в том отношении, что атом водорода расположен посредине между двумя тяжелыми атомами. Обычно энергии водородных связей намного меньше, чем для иона дифторида, а водород более тесно связан с одним из атомов, чем с другим, как в димере муравьиной кислоты (рис. 1.1). В действительности геометрия двух компонентов, составляющих комплекс, немного отличается от их геометрии в изолированных состояниях .
Таблица 1.1 Энергии димеризации некоторых газофазных димеров с водородной связью
| Димер | Энергия димеризации, кДж/моль -1 |
| 29±4 | |
| 22±6 | |
| 19±2 | |
| 9±1 | |
| 7±1 |





Обнаружено смещение кислотно-основного равновесия молекулярный комплекс ионная пара вправо при повышении полярности растворителя. Кроме указанных фиксируются и другие структурные и спектроскопические особенности водородных связей, которые используются, с одной стороны, для идентификации последних, а с другой – в расшифровке их электронной природы. Так как водородная связь возникает только в том...





Водородную связь от межмолекулярной. Если спектрально фиксируется образование Н-связей, а признаков ассоциации нет, это верное указание на внутримолекулярный характер водородной связи. Кроме того, межмолекулярная Н-связь (и ее спектральное проявление) исчезает при низкой концентрации вещества в нейтральном растворителе, тогда как внутримолекулярная Н-связь в этих условиях сохраняется. Водородные...
Длин химических связей молекулы растворителя, дипольный момент молекулы растворителя и вязкость, выражается следующим уравнением (2) Коэффициент множественной регрессии составляет КММР = 0,999. В табл. 2 представлены значения энергии водородных связей в различных растворителях, полученные по ур. (1) и (2), в сравнении с литературными данными. Таблица 2 Величины энергии водородных связей...


По их поведению в растворах на две категории: а) вещества, растворы которых обладают ионной проводимостью (электролиты); б) вещества, растворы которых не обладают ионной проводимостью (неэлектролиты). К электролитам относится большинство неорганических кислот, оснований и солей. К неэлектролитам относятся многие органические соединения, например спирты, углеводы. Электролитическая диссоциация. ...
В молекулах соединениях HF, H 2 O, NH 3 существуют связи водорода с сильно электроотрицательным элементом (Н–F, Н–O, Н–N). Между молекулами таких соединений могут образовываться межмолекулярные водородные связи . В некоторых органических молекулах, содержащих связи Н–O, Н–N, могут возникать внутримолекулярные водородные связи .
Механизм образования водородной связи имеет частично электростатический, частично донорно – акцепторный характер. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором - атомы водорода, соединенные с этими атомами. Как и для ковалентной связи, для водородной связи характерны направленность в пространстве и насыщаемость .
Водородную связь принято обозначать точками: Н ··· F. Водородная связь проявляется тем сильнее, чем больше электроотрицательность атома-партнера и чем меньше его размеры. Она характерна прежде всего для соединений фтора, а также кислорода, в меньшей степени азота, в еще меньшей степени для хлора и серы. Соответственно меняется и энергия водородной связи (табл. 1).
Таблица 1. Средние значения энергий водородных связей
Межмолекулярная и внутримолекулярная водородная связь
Благодаря водородным связям молекулы объединяются в димеры и более сложные ассоциаты. Молекулы воды образуют ассоциаты (Н 2 О) 2 , (Н 2 О) 3 , (Н 2 О) 4 ; спирта (C 2 H 5 ОН) 4 . Этим и объясняется увеличение температуры кипения спиртов по сравнению с углеводородами, Наблюдается хорошее растворение метанола и этанола в воде. Водородная связь, возникшая между молекулами, называется межмолекулярной.
Например, образование димера парагидроксибензальдегида можно представить следующей схемой (рис. 1).
Рис. 1. Образование межмолекулярных водородных связей в парагидроксибензальдегиде.
Водородные связи могут возникать как между различными молекулами (межмолекулярная водородная связь), так и внутри молекулы (внутримолекулярная водородная связь). Внутримолекулярные водородные связ и имеются в многоатомных спиртах, углеводах, белках и других органических веществах.
Влияние водородной связи на свойства веществ
Наиболее удобным индикатором существования межмолекулярной водородной связи является температура кипения вещества. Более высокая температура кипения воды (100 o C по сравнению с водородными соединениями элементов подгруппы кислорода (H 2 S, H 2 Se, H 2 Te) объясняется наличием водородных связей: на разрушение межмолекулярных водородных связей в воде необходимо затратить дополнительную энергию.
Водородная связь существенным образом может влиять на структуру и свойства веществ. Существование межмолекулярной водородной связи повышает температуры плавления и кипения веществ. Наличие внутримолекулярной водородной связи приводит к тому, что молекула дезоксирибонуклеиновой кислоты (ДНК) оказывается свернутой в воде двойной спирали.
Водородная связь также играет важную роль в процессах растворения, поскольку растворимость зависит и от способности соединения давать водородные связи с растворителем. В результате содержащие ОН-группы такие вещества, как сахар, глюкоза, спирты, карбоновые кислоты, как правило, хорошо растворимы в воде.
Примеры соединений: одноатомные (метанол, этанол) и многоатомные спирты (глицерин, этиленгликоль), карбоновые кислоты, амины, аминокислоты, белки, вода, аммиак, фтороводород, кислородсодержащие карбоновые кислоты.













