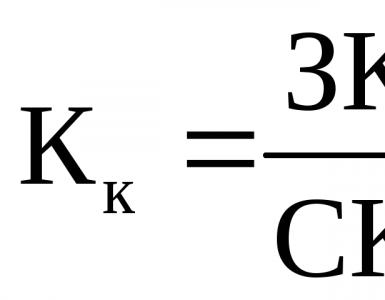Химическое уравнение
Хорошей аналогией химических реакций служит процесс выпекания печенья. Вы смешиваете ингредиенты (муку, масло, соль, сахар, яйца), и после выпекания смесь превращается в нечто новое (печенье). В химических терминах уравнение – это рецепт, ингредиенты выступают в роли "реагентов", а печенье соответствует "продуктам" реакции. Все химические уравнения имеют форму "A + B --> C (+ D..)", где каждая буква обозначает химический элемент или молекулу (соединение атомов, удерживаемых вместе химическими связями). Стрелка указывает на реакцию, то есть изменение.
Шаги
Часть 1
Некоторые основные понятия химии-
Освойте правильную запись молекул. Запись молекулы представляет собой последовательный перечень атомов элементов, составляющих молекулу, причем после каждого символа стоит число в виде нижнего индекса, указывающее на количество атомов данного типа в молекуле. Если атом один, число опускается.
- Например, молекула метана состоит из 1 атома углерода и 4 атомов водорода, поэтому она записывается как CH4. Схожим образом обозначаются и другие молекулы, например, молекулы аммиака (NH3) и хлорной извести (HClO4), широко используемых в быту.
Изучите периодическую таблицу элементов. Атомы – это базовые строительные кирпичики в химии. Периодическая таблица, называемая также таблицей Менделеева, содержит все известные атомы (элементы). Периодическая система элементов есть в большинстве учебников по химии, ее легко можно найти в Интернете. В этой таблице содержится большое количество информации. Вы найдете в ней атомный номер (число протонов в ядре атома), атомную массу (сумму протонов и нейтронов, составляющих атомное ядро) и атомный символ элемента.
Чистые элементы могут существовать в виде нескольких веществ, или модификаций. Например, чистый углерод, обозначаемый буквой С, может образовывать графит либо алмаз.
Часть 2
Запись химических реакцийЧасть 3
Балансировка химических уравнений-
Помните о сохранении атомов. При химических реакциях не могут создаваться новые атомы или разрушаться старые (в отличие от ядерных реакций, рассмотрение которых выходит за рамки данной статьи), поэтому в левой и правой частях уравнения (слева и справа от стрелки) будут присутствовать одни и те же атомы в одинаковом количестве.
- Например, уравнение ржавления железа в виде Fe + O2 --> Fe2O3 не может быть правильным. В реакцию вступают 1 атом Fe и 2 атома O, а в результате получаются 2 атома Fe и 3 атома O. Чтобы исправить это, следует учесть количество и соотношение атомов реагентов и продуктов реакции. Путем простых вычислений можно определить, что правильная запись уравнения имеет вид 4 Fe + 3 O2 --> 2 Fe2O3. Теперь с обеих сторон уравнения находятся четыре атома железа и шесть атомов кислорода. В химических уравнениях следует использовать целые числа: поскольку не существует половинок молекул, запись 2 Fe + 11/2 O2 --> Fe2O3 будет неверной.
Уравнение химической реакции даёт качественную и количественную информацию о химической реакции, реагентах и продуктах реакции; его составление основывается на законах стехиометрии , в первую очередь, законе сохранения массы веществ в химических реакциях. Кроме уравнений используются полные и краткие схемы химических реакций - условные записи, дающие представление о природе реагентов и продуктов, то есть качественную информацию о химической реакции.
O 2 + 2 H 2 → 2 H 2 O
История
Сначала не было представления о химических уравнениях, ещё не были известны основные химические законы, но уже в алхимический период развития химии начали обозначать химические элементы символами.
С дальнейшим развитием химии менялись представления о символике химических элементов ,ской записи, используя химические формулы . Первым предложил использовать химические уравнения Жан Бегун (Jean Beguin) в 1615 году в одном из первых учебников по химии Tyrocinium Chymicum («Начала химии» ).
Конец XVIII-начало XIX вв. - становление законов стехиометрии . У истоков этих исследований стоял немецкий ученый И. В. Рихтер . В студенческие годы на него большое впечатление произвели слова его учителя - философа И. Канта о том, что в отдельных направлениях естественных наук истинной науки столько, сколько в ней математики. Рихтер посвятил свою диссертацию использованию математики в химии. Не будучи в сущности химиком, Рихтер ввел первые количественные уравнения химических реакций, стал использовать термин стехиометрия .
Правила составления
Для составления уравнений химических реакций, кроме знания формул реагентов и продуктов реакции, необходимо верно подобрать коэффициенты. Это можно сделать, используя несложные правила . В левой части уравнения записывают формулы (формулу) веществ, вступивших в реакцию, соединяя их знаком «плюс». В правой части уравнения записывают формулы(формулу) образовавшихся веществ, также соединенных знаком «плюс». Между частями уравнения ставят знак равенства или стрелку. Затем находят коэффициенты - числа, стоящие перед формулами веществ, чтобы число атомов одинаковых элементов в левой и правой частях уравнения было равным.
Для обозначения различных типов реакций используются следующие символы:
Запись ионных уравнений
Ионные уравнения - это химические уравнения, в которых
Схема химической реакции.
Существует несколько способов записи химических реакций. Co «словесной» схемой реакции вы ознакомились в § 13.
Приводим еще один пример:
сера + кислород -> сернистый газ.
Ломоносов и Лавуазье открыли закон сохранения массы веществ при химической реакции. Он формулируется так:
Объясним, почему массы пепла и прокаленной меди отличаются от масс бумаги и меди до ее нагревания.
В процессе горения бумаги принимает участие кислород, который содержится в воздухе (рис. 48, а).
Следовательно, в реакцию вступают два вещества. Кроме пепла, образуются углекислый газ и вода (в виде пара), которые попадают в воздух и рассеиваются.

Рис. 48. Реакции бумаги (а) и меди (б) с кислородом
Антуан-Лоран Лавуазье (1743-1794)

Выдающийся французский химик, один из основателей научной химии. Академик Парижской академии наук. Ввел в химию количественные (точные) методы исследования. Экспериментально определил состав воздуха и доказал, что горение - это реакция вещества с кислородом, а вода - соединение Гидрогена с Оксигеном (1774- 1777).
Составил первую таблицу простых веществ (1789), предложив фактически классификацию химических элементов. Независимо от М. В. Ломоносова открыл закон сохранения массы веществ при химических реакциях.

Рис. 49. Опыт, подтверждающий закон Ломоносова - Лавуазье:а - начало опыта; б - окончание опыта
Их масса превышает массу кислорода. Поэтому масса пепла меньше массы бумаги.
При нагревании меди кислород воздуха «соединяется» с ней (рис. 48, б). Металл превращается в вещество черного цвета (его формула - CuO, а на звание - купрум(П) оксид). Очевидно, что масса продукта реакции должна превышать массу меди.
Прокомментируйте опыт, изображенный на рисунке 49, и сделайте вывод.
Закон как форма научных знаний.
Открытие законов в химии, физике, других науках происходит после проведения учеными многих экспериментов и анализа полученных результатов.
Закон - это обобщение объективных, независимых от человека связей между явлениями, свойствами и т. д.
Закон сохранения массы веществ при химической реакции - важнейший закон химии. Он распространяется на все превращения веществ, которые происходят и в лаборатории, и в природе.
Химические законы дают возможность прогнозировать свойства веществ и протекание химических реакций, регулировать процессы в химической технологии.
Для того чтобы объяснить закон, выдвигают гипотезы, которые проверяют с помощью соответствующих экспериментов. Если одна из гипотез подтверждается, на ее основе создают теорию. В старших классах вы ознакомитесь с несколькими теориями, которые разработали ученые-химики.
Общая масса веществ при химической реакции не изменяется потому, что атомы химических элементов во время реакции не возникают и не исчезают, а происходит только их перегруппировка. Другими словами,
количество атомов каждого элемента до реакции равно количеству его атомов после реакции. На это указывают схемы реакций, приведенные в начале параграфа. Заменим в них стрелки между левыми и правыми частями на знаки равенства:
Такие записи называют химическими уравнениями.
Химическое уравнение - это запись химической реакции с помощью формул реагентов и продуктов, которая согласуется с законом сохранения массы веществ.
Существует много схем реакций^ которые не соответствуют закону Ломоносова - Лавуазье.
Например, схема реакции образования воды:
H 2 + O 2 -> H 2 O.
В обеих частях схемы содержится одинаковое количество атомов Гидрогена, но разное количество атомов Оксигена.
Превратим эту схему в химическое уравнение.
Для того чтобы в правой части было 2 атома Оксигена, поставим перед формулой воды коэффициент 2:
H 2 + O 2 -> H 2 O.
Теперь справа стало четыре атома Гидрогена. Чтобы такое же количество атомов Гидрогена было и в левой части, запишем перед формулой водорода коэффициент 2. Получаем химическое уравнение:
2Н 2 + O 2 = 2Н 2 0.
Таким образом, чтобы превратить схему реак ции в химическое уравнение, нужно подобрать коэффициенты для каждого вещества (в случае необходимости), записать их перед химическими формулами и заменить стрелку на знак равенства.
Возможно, кто-то из вас составит такое уравнение: 4Н 2 + 20 2 = 4Н 2 0. В нем левая и правая части содержат одинаковые количества атомов каждого элемента, но все коэффициенты можно уменьшить, разделив на 2. Это и следует сделать.
Это интересно
Химическое уравнение имеет много общего с математическим.
Ниже представлены различные способы записи рассмотренной реакции.

Превратите схему реакции Cu + O 2 -> CuO в химическое уравнение.
Выполним более сложное задание: превратим в химическое уравнение схему реакции
В левой части схемы - I атом Алюминия, а в правой - 2. Поставим перед формулой металла коэффициент 2:
Атомов Сульфура справа в три раза больше, чем слева. Запишем в левой части перед формулой соединения Сульфура коэффициент 3:
Теперь в левой части количество атомов Гидрогена равно 3 2 = 6, а в правой - только 2. Для того чтобы и справа их было 6, поставим перед формулой водорода коэффициент 3 (6: 2 = 3):
Сопоставим количество атомов Оксигена в обеих частях схемы. Они одинаковы: 3 4 = 4 * 3. Заменим стрелку на знак равенства:
Выводы
Химические реакции записывают с помощью схем реакций и химических уравнений.
Схема реакции содержит формулы реагентов и продуктов, а химическое уравнение - еще и коэффициенты.
Химическое уравнение согласуется с законом сохранения массы веществ Ломоносова - Лавуазье:
масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции.
Атомы химических элементов во время реакций не появляются и не исчезают, а происходит лишь их перегруппировка.
?
105. Чем отличается химическое уравнение от схемы реакции?
106. Расставьте пропущенные коэффициенты в записях реакций:
107. Превратите в химические уравнения такие схемы реакций:
108. Составьте формулы продуктов реакций и соответствующие химические уравнения:
109. Вместо точек запишите формулы простых веществ и составьте хими ческие уравнения:
Примите во внимание, что бор и углерод состоят из атомов; фтор, хлор, водород и кислород - из двухатомных молекул, а фосфор (белый) - из четырехатомных молекул.
110. Прокомментируйте схемы реакций и превратите их в химические уравнения:
111. Какая масса негашеной извести образовалась при длительном прока ливании 25 г мела, если известно, что выделилось 11 г углекислого газа?
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. - К.: ВЦ «Академія», 2008. - 136 с.: іл.
Содержание урока конспект урока и опорный каркас презентация урока интерактивные технологии акселеративные методы обучения Практика тесты, тестирование онлайн задачи и упражнения домашние задания практикумы и тренинги вопросы для дискуссий в классе Иллюстрации видео- и аудиоматериалы фотографии, картинки графики, таблицы, схемы комиксы, притчи, поговорки, кроссворды, анекдоты, приколы, цитаты Дополнения рефераты шпаргалки фишки для любознательных статьи (МАН) литература основная и дополнительная словарь терминов Совершенствование учебников и уроков исправление ошибок в учебнике замена устаревших знаний новыми Только для учителей календарные планы учебные программы методические рекомендации